近日,福莱明生物传来重大喜讯:其递交的多项医疗器械注册文件正式通过美国食品药品监督管理局(FDA)审核,顺利完成全系列产品注册与列名。这一突破性进展,标志着福莱明生物正式斩获进入以美国为代表的欧美国际市场的 “准入密钥”,在生物科技全球化征程中树立重要里程碑。

作为一家聚焦重组功能蛋白等合成生物新材料的高新技术企业,福莱明生物依托与中科院过程工程研究所共建的重组蛋白关键共性技术生物合成平台,构建了覆盖创新生物材料、医疗器械、美妆、日用等领域的生物医药大健康全产业链布局。企业凭借国内少数兼具自主知识产权生物原材料研发能力、生物合成技术开发能力及终端产品生产能力的全链条优势,以 “AI 设计 + 生物合成” 双轮驱动,持续智造 “重组融合蛋白” 核心技术,为生物科技新质生产力发展注入源头活水。
美国食品药品监督管理局(FDA)作为国际权威监管机构,由医生、微生物学家、药理学家等多领域专家组成,肩负着保障食品、药品、医疗器械等产品安全的重要职责,其标准被全球多国视为品质 “金标杆”。对于企业而言,FDA 注册是产品进入美国市场的法定前提,更是叩开全球主流市场的 “敲门砖”——WTO 成员国普遍认可 FDA 认证,其国际自由销售许可证被视作食品药品领域的最高通行资质。
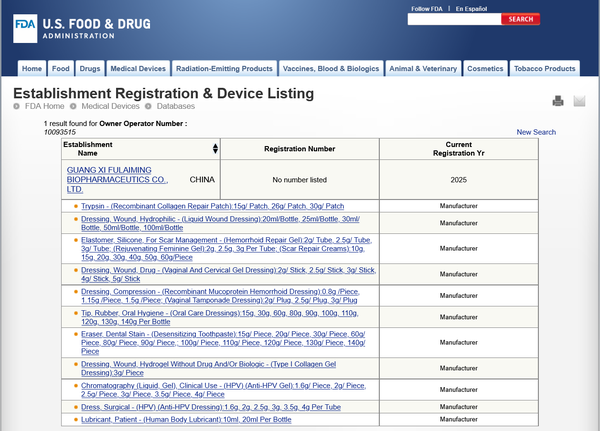
福莱明生物的核心技术成果 —— 重组人源化胶原蛋白(FHTFF 福活因子、福活肽)与重组类胶原生物防御蛋白(PHPV 融合因子、融合肽),早已实现国内外认证体系的 “双轨突破”:国内获国家发明专利、NMPA 原材料主文档登记;国际被国际基因蛋白数据库收录、获 INCI 国际化妆品目录标准名称,衍生医疗器械均通过 NMPA 注册。此次 FDA 510 (k) waiver注册列名的成功,意味着其产品安全性与有效性获得中美监管体系的双重背书。注册信息显示,产品企业代码、列名号、监管编号等关键数据已完整录入 FDA 数据库,为后续出口清关等流程筑牢合规根基。
“FDA 认证是全球生物医药领域的品质试金石。” 福莱明生物创始人易祥表示,国际市场对 FDA 认证产品的高度信任,不仅源于其严格的审核机制,更因其标准被近百个国家作为产品商业化临床应用的前提。此次注册成功,不仅让福莱明生物产品可合法进入美国及 WTO 成员国市场,更显著提升了品牌在国际竞争中的 “信任溢价”。
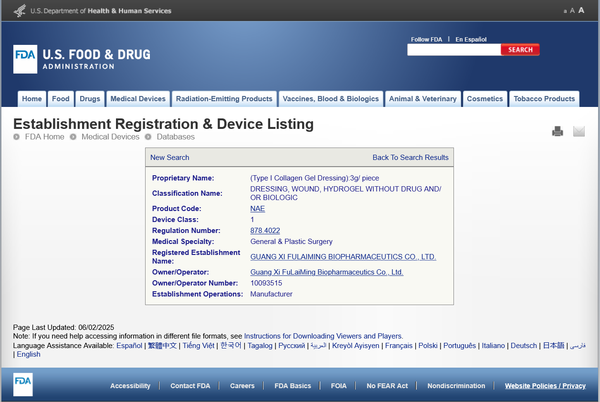
(FHTFF福活肽--重组人源化胶原蛋白衍生产品 I 型胶原凝胶敷料FDA注册信息页面)
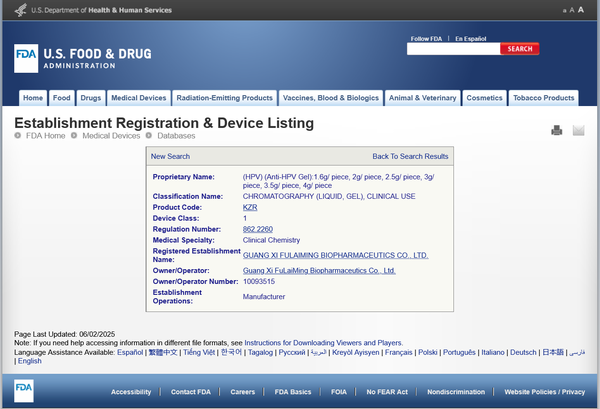
(PHPV融合肽--重组类胶原蛋白衍生产品PHPV卡拉胶凝胶FDA注册信息页面)
展望未来,福莱明生物将以此次突破为起点,加速推进欧盟 CE 认证、东盟市场准入等全球化布局,并计划与美欧地区代理商合作,构建本地化营销网络。企业的目标不仅是 “走出去”,更要 “走得远”—— 通过持续的技术创新与合规布局,让 “中国智造” 的重组蛋白生物科技产品在全球大健康市场占据更重要的位置。
此次 FDA 注册的圆满完成,既是福莱明生物技术实力与创新能力的集中展现,更是中国生物科技企业参与国际竞争的生动范本。随着全球化战略的深入实施,福莱明生物将继续以合成生物新材料为核心,推动更多优质产品走向世界,为全球生物科技发展贡献中国方案与中国力量。
责任编辑:夏岩










